Cơ Sở Khoa Học của Phản Ứng Zn + AgNO3
Bản Chất Phản Ứng
Phản ứng giữa kẽm (Zn) và bạc nitrat (AgNO3) là một phản ứng oxi hóa – khử điển hình trong hóa học vô cơ. Phương trình phản ứng tổng quát:
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag↓
Trong đó:
- Zn đóng vai trò chất khử (bị oxi hóa): Zn → Zn2+ + 2e-
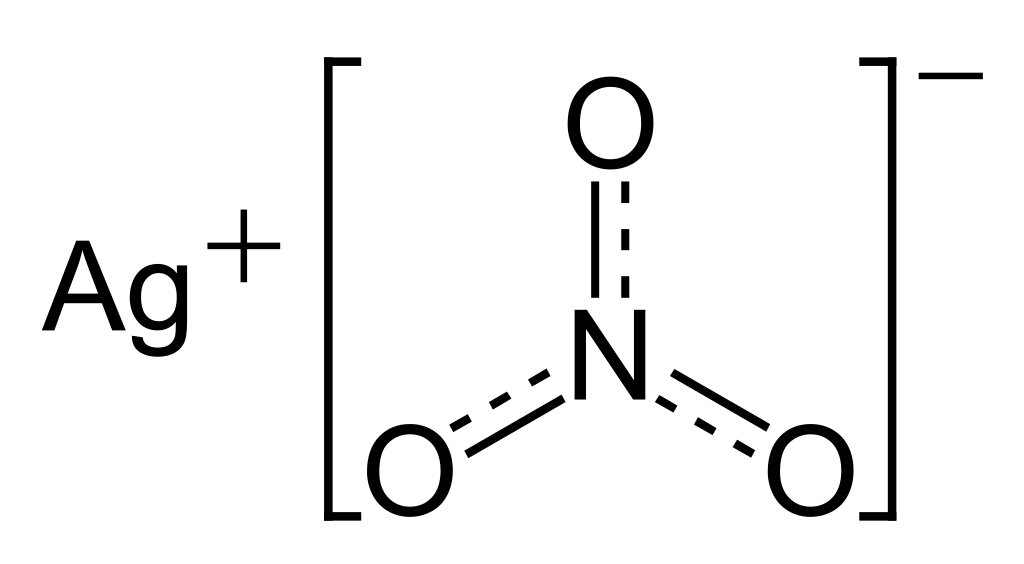
- Ag+ đóng vai trò chất oxi hóa (bị khử): 2Ag+ + 2e- → 2Ag
Điều Kiện Phản Ứng
- Nhiệt độ:
- Phản ứng xảy ra tốt ở nhiệt độ phòng (25°C)
- Tốc độ phản ứng tăng khi nhiệt độ tăng
- Nhiệt độ tối ưu: 30-40°C
- Nồng độ:
- Nồng độ AgNO3 thích hợp: 0.1M – 1M
- Tỷ lệ mol tối ưu Zn:AgNO3 = 1:2
- Môi trường:
- pH tối ưu: 5-7
- Không khí không ảnh hưởng đến phản ứng
- Cần dung môi là nước
Ứng Dụng Thực Tiễn của Phản Ứng
Trong Công Nghiệp
- Sản Xuất Bạc Tinh Khiết:
- Tách bạc từ quặng
- Tinh chế bạc công nghiệp
- Sản xuất bạc nano
- Mạ Kim Loại:
- Mạ bạc trang sức
- Phủ lớp bảo vệ chống ăn mòn
- Tạo lớp phủ dẫn điện
- Điện Tử:
- Sản xuất mạch in
- Chế tạo cảm biến
- Làm vật liệu dẫn điện
Trong Y Học
- Sản Xuất Thuốc:
- Tổng hợp hợp chất bạc kháng khuẩn
- Chế tạo thuốc khử trùng
- Sản xuất thuốc điều trị vết thương
- Thiết Bị Y Tế:
- Phủ lớp bạc kháng khuẩn
- Chế tạo dụng cụ phẫu thuật
- Sản xuất vật liệu cấy ghép
Trong Nghiên Cứu và Giáo Dục
- Thí Nghiệm Giáo Dục:
- Minh họa phản ứng oxi hóa – khử
- Nghiên cứu động học phản ứng
- Thực hành kỹ thuật phòng thí nghiệm
- Nghiên Cứu Khoa Học:
- Phát triển vật liệu mới
- Nghiên cứu xúc tác
- Tổng hợp nano bạc

Các Yếu Tố Ảnh Hưởng đến Hiệu Suất Phản Ứng
Yếu Tố Vật Lý
- Diện Tích Bề Mặt:
- Kẽm dạng bột phản ứng nhanh hơn dạng thanh
- Bề mặt càng sạch, phản ứng càng hiệu quả
- Cần loại bỏ lớp oxit bề mặt
- Khuấy Trộn:
- Tăng tốc độ phản ứng
- Giúp sản phẩm đồng đều
- Tránh tích tụ cục bộ
Yếu Tố Hóa Học
- Độ Tinh Khiết:
- Kẽm càng tinh khiết, hiệu suất càng cao
- AgNO3 không nhiễm tạp chất
- Nước cất hoặc deion
- Chất Ức Chế/Xúc Tác:
- Một số ion kim loại có thể ức chế phản ứng
- Acid nitric làm tăng tốc độ phản ứng
- pH ảnh hưởng đến cơ chế phản ứng

Phương Pháp Tối Ưu Hóa Phản Ứng
Quy Trình Chuẩn
- Chuẩn Bị:
- Làm sạch bề mặt kẽm
- Pha dung dịch AgNO3 đúng nồng độ
- Kiểm tra nhiệt độ và pH
- Thực Hiện:
- Nhúng kẽm vào dung dịch
- Duy trì khuấy đều
- Theo dõi thời gian phản ứng
- Thu Hồi Sản Phẩm:
- Lọc tách bạc
- Rửa sạch sản phẩm
- Sấy khô và bảo quản
Kiểm Soát Chất Lượng
- Các Chỉ Tiêu:
- Độ tinh khiết của bạc
- Kích thước hạt
- Hiệu suất phản ứng
- Phương Pháp Phân Tích:
- Phân tích XRD
- Kính hiển vi điện tử
- Phân tích khối lượng
Thông Tin Thêm và Liên Hệ
Để biết thêm thông tin về các khóa học thực hành và workshop liên quan đến phản ứng hóa học, vui lòng liên hệ:
Global Citizen – AIESEC Hanoi
Hotline: 0912 13 13 13
Email: [email protected]
Website: aiesechanoi.org
Bài viết được phát triển bởi đội ngũ chuyên môn của AIESEC Hanoi nhằm cung cấp kiến thức chuyên sâu về phản ứng Zn + AgNO3 và ứng dụng thực tiễn của nó trong công nghiệp và đời sống.
